A chuva ácida é um termo usado para descrever a precipitação que tem um valor de pH inferior a cerca de 5,5 devido à ação de várias substâncias químicas .
A chuva torna-se ácida principalmente pela absorção de nitrogênio e dióxido de enxofre (veja também ácidos ), que são liberados como subprodutos quando os combustíveis fósseis são queimados em sistemas de aquecimento e veículos. A chuva ácida é considerada uma das principais causas de morte das florestas, pois danifica diretamente as plantas e altera suas condições de crescimento, alterando quimicamente o solo.
Óxidos de enxofre e nitrogênio são liberados no ar durante a combustão de fontes de energia sulfurosa, como petróleo, gás natural ou carvão. Devido ao aumento de residências, bem como ao crescimento do tráfego e da indústria, as quantidades dessas substâncias químicas também estão aumentando. O dióxido de enxofre combina-se com outras substâncias na atmosfera para formar vários ácidos, principalmente nítrico e sulfúrico. Na atmosfera, os ácidos sulfurosos são absorvidos pela chuva, mas também pela neve, granizo e neblina, e assim chegam ao solo, onde se infiltram na terra e se depositam nas folhas das plantas.
A chuva ácida simplesmente explicada
Pense na chuva ácida como precipitação com pH abaixo de 5,5. Isso significa que o valor do pH da chuva ácida está abaixo do valor da chuva normal, que é 5,5 – 5,7. O pH é uma medida de se uma solução é básica ou ácida. Quanto menor o pH, mais ácida a solução.

A chuva ácida é formada principalmente quando poluentes emitidos (por exemplo, de usinas de energia) se combinam com a água nas nuvens. Isso diminui o pH da água. As nuvens também podem transportar esse composto químico para regiões distantes e liberá-lo lá.
A chuva ácida pode ter um impacto negativo em corpos d’água, plantas e edifícios, entre outras coisas.Definição
A chuva ácida refere-se à precipitação com pH abaixo do pH da água da chuva pura. Abaixo de um pH de 5,5, é considerado ácido. Suas propriedades ácidas podem ter um impacto negativo em toda a biosfera.
Formação de chuva ácida
Basicamente, a chuva ácida ocorre em conexão com óxidos de nitrogênio (NO X ) ou óxidos de enxofre (SO X ) como o dióxido de enxofre (SO 2 ).
Causas da chuva ácida
A maior causa da chuva ácida é a poluição do ar . Isso faz com que a composição do ar mude. No entanto, como as atividades humanas poluíram a atmosfera nas últimas décadas, o ar impuro é agora a norma. Portanto, o “grau de poluição do ar” é o principal responsável pela chuva ácida.
As causas da poluição do ar são variadas. Os seguintes setores são os principais responsáveis por isso:
- Indústria (especialmente a combustão de combustíveis fósseis como o petróleo)
- Transporte (por exemplo, carros e aviação)
- residências particulares (por exemplo, aquecimento e iluminação)
- Agricultura (por exemplo, pesticidas)
Nestes setores em particular, os poluentes são emitidos na forma de partículas sólidas, gases ou aerossóis.
Mas a chuva ácida também pode se formar nas proximidades de vulcões ativos. Muitos gases escapam aqui durante a erupção, incluindo dióxido de enxofre em particular. Isso pode combinar com a chuva.

Fórmula da chuva ácida
Você também pode descrever a formação da chuva ácida com uma equação de reação química. Como você já sabe, ele pode se formar por um lado através da conexão com óxidos de enxofre (SO X ) como o dióxido de enxofre e por outro lado através da conexão com óxidos de nitrogênio (NO X ).
O dióxido de enxofre ( SO 2 ) se forma quando o enxofre (S) entra na atmosfera e se combina com o oxigênio (O 2 ):

Algumas moléculas de dióxido de enxofre podem se combinar com oxigênio novamente para formar trióxido de enxofre ( SO 3 ):
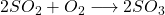
Dióxido de enxofre e trióxido de enxofre dissolvem-se em água e formam ácido sulfuroso (H 2 SO 3 ) ou ácido sulfúrico (H 2 SO 4 ):
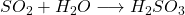
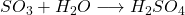
Quanto maior a concentração desses ácidos na água da nuvem, mais ácida é a chuva, ou seja, menor o valor do pH.
Em altas temperaturas, especialmente na indústria, óxidos de nitrogênio como o dióxido de nitrogênio (NO 2 ) podem se formar. Para fazer isso, o nitrogênio ( N 2
) contido no ar primeiro se combina com o oxigênio para formar monóxido de nitrogênio (2NO):

O óxido nítrico combina-se com o oxigênio para formar dióxido de nitrogênio. Na fase gasosa, também está presente como tetróxido de dinitrogênio (N 2 O 4 ):

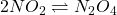
NO 2 e N 2 O 4 agora podem reagir com água para formar ácido nitroso (HNO 2 ) e ácido nítrico (HNO 3 ):
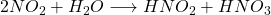

Efeitos da chuva ácida
A chuva ácida pode ter uma variedade de efeitos. Em particular, corpos de água, plantas e solo, bem como edifícios, são severamente afetados.
Efeitos em corpos d’água
Quando a chuva ácida cai em uma grande variedade de corpos d’água, ela pode fazer com que seus níveis de pH caiam drasticamente. O valor do pH das águas naturais pode variar entre 6,5 e 8,5 em alguns casos.
A chuva ácida pode trazer o pH abaixo desse nível, prejudicando ou até matando pequenas criaturas e plantas. Além disso, os íons metálicos tóxicos , que também são muito prejudiciais, podem se acumular melhor no ambiente ácido .
No geral, esse baixo valor de pH pode, por exemplo , inibir processos metabólicos por um longo período de tempo ou reduzir a biodiversidade .
efeitos nas plantas
As plantas obtêm a maior parte de seus nutrientes do solo. Quando o solo se torna ácido, os íons metálicos tóxicos se acumulam novamente, dificultando a absorção de nutrientes e o crescimento das plantas. Além disso, as plantas são muito mais suscetíveis a várias doenças.
Durante um longo período de tempo, o solo acidificado pode até levar à morte de florestas inteiras (= floresta morta ).
Efeitos em edifícios
Não só a natureza, mas também alguns edifícios podem ser danificados pela chuva ácida. Acima de tudo, arenito, calcário, concreto ou mármore podem ser atacados pelo ácido. Devido a este dano ácido, o intemperismo (= decomposição da rocha) dos edifícios começa mais rápido e mais reparos são necessários.
Muitos edifícios e estátuas históricas, como o Taj Mahal na Índia ou a Acrópole em Atenas, que foram afetados pela chuva ácida por muito tempo, sofrem danos significativos.
Medidas preventivas para chuva ácida
Devido às graves consequências da chuva ácida, é importante iniciar as contramedidas em um estágio inicial. Você pode tratar os sintomas ou corrigir as causas diretamente.
Embora o tratamento dos sintomas seja relativamente fácil, mas de curto prazo, o tratamento das causas pode trazer melhorias a longo prazo.
Medidas contra os sintomas
Para aliviar os sintomas, a cal é espalhada de helicóptero em muitas áreas da Europa. Este calcário é capaz de elevar o pH do solo e melhorar a estrutura do solo. Por exemplo, pode aumentar a capacidade de armazenamento de água do solo e melhorar a aeração, o que facilita o crescimento das raízes.
Medidas contra as causas
A primeira ação contra as causas da chuva ácida ocorreu na Alemanha na década de 1980. Foi introduzido como regra que em grandes usinas de energia fóssil os gases de saída devem ser dessulfurizados . Como resultado, menos óxidos de enxofre (SO x ) entraram na atmosfera e os ácidos sulfúricos foram mais difíceis de formar. Em motores de combustão interna, como os de carros ou aviões, o enxofre é removido diretamente do combustível antes de ser usado.
Enquanto a remoção de óxidos de enxofre é relativamente fácil, a remoção de óxidos de nitrogênio é muito mais difícil. Isso se deve principalmente ao fato de que o ar consiste em grande parte de nitrogênio (aprox. 78%).
Efeitos da chuva ácida no meio ambiente
Em muitos casos, os danos florestais em grande escala podem ser atribuídos aos efeitos dos ácidos sulfurosos. Se estes entrarem no solo, eles alteram o equilíbrio químico lá, que fornece às plantas sua base de vida. A acidificação do solo altera principalmente a composição sensível de nutrientes e o equilíbrio hídrico, o que leva a danos nas raízes finas das árvores. Especialmente a liberação de alumínio e os metais pesados são responsáveis pela morte em massa das plantas. Prejudicam as funções naturais das raízes finas e do micélio que as envolve. Como resultado, as árvores não podem mais absorver nutrientes vitais, ou apenas de forma limitada. A longo prazo, o déficit de nutrientes resultante faz com que a árvore perca sua resistência e se torne suscetível a doenças e influências externas.
Não apenas pragas como besouros e doenças fúngicas têm facilidade com as árvores enfraquecidas. A falta de nutrientes também torna o tecido mais sensível e resseca. Isso se deve à ação direta dos ácidos contidos na chuva, que aderem às folhas e agulhas e aí prejudicam a função dos chamados estômatos. Se estes não puderem mais fechar devido a depósitos de ácido, os estômatos tornam-se rígidos. A árvore não pode mais armazenar umidade no interior e seca gradualmente. Uma tempestade ou tempestade pode rapidamente causar sérios danos ao tronco e galhos de uma árvore tão doente, pois a substância se torna porosa e quebradiça.
Enquanto a chuva ácida pode levar a vários padrões de doenças em plantas e causar a morte de áreas inteiras de floresta, corpos d’água e os animais que vivem neles também são severamente danificados por seus efeitos. O valor de pH alterado leva à dissolução de conchas calcárias e conchas de moluscos, altera as condições de crescimento das plantas na água e priva muitos animais de sua fonte de alimento. Portanto, a chuva ácida não está associada apenas à morte das florestas, mas também à redução da biodiversidade relacionado. Além disso, o rápido desgaste das edificações também se deve à ação da chuva ácida.
Medidas contra a chuva ácida
Em regiões onde grandes depósitos de rocha calcária existem, os efeitos são muito menores porque a cal neutraliza amplamente os ácidos. Por esta razão, grandes quantidades de cal estão espalhadas em muitos países europeus hoje para proteger a paisagem da acidificação. No entanto, é essencial reduzir drasticamente a emissão de toxinas, o que é assegurado principalmente pela instalação de sistemas de filtragem em sistemas de aquecimento industrial e veículos. O descomissionamento de usinas que utilizam combustíveis fósseis para gerar eletricidade, o uso de energias renováveis e o uso econômico da energia em geral são medidas importantes no combate à acidificação do meio ambiente.
Resumo
- A principal causa da chuva é feita pelo homem. Quando o gás natural, carvão mineral ou petróleo é queimado, dióxido de enxofre e nitrogênio são liberados na atmosfera. As gotas de chuva ligam essas substâncias, caem no solo e, assim, acidificam o solo.
- A chuva ácida danifica tanto as plantas (palavra-chave: morte da floresta) quanto os corpos d’água
- A chuva ácida é a precipitação com pH abaixo de 5,5
- É criado pela combinação de água com poluentes como óxidos de nitrogênio e óxidos de enxofre
- As propriedades ácidas podem ter um efeito negativo em corpos de água, plantas e edifícios, entre outras coisas
- Contramedidas podem ser tomadas contra os sintomas ou diretamente contra as causas
chuva ácida
Como se forma a chuva ácida?
A chuva ácida é causada por reações químicas nas quais óxidos de nitrogênio ou óxidos de enxofre se combinam com a água do ar para formar ácido sulfúrico ou nítrico.
Quão perigosa é a chuva ácida?
A chuva ácida tem vários efeitos negativos sobre o meio ambiente. Afetados são, por exemplo, plantas, florestas, massas de água, mas também edifícios feitos pelo homem.
Quando começou o problema da chuva ácida?
O problema da chuva ácida surgiu principalmente na década de 1980 devido à queima de combustíveis fósseis em usinas de energia. Isso liberou grandes quantidades de enxofre na atmosfera.
O que acontece na chuva ácida?
A chuva ácida é caracterizada por um pH ácido abaixo de 5,5, o que tem efeitos negativos em vários ecossistemas.